2016年曲靖市教育系统公开招聘教师考试
专业知识 教法技能 大纲
化学(高中教育岗位)
曲靖市教育局
一、考试性质
曲靖市教育系统公开招聘教师考试属选拔性考试。教育行政部门根据教育事业改革和发展的需要,考查、考核考生从事教师工作的专业知识、教育教学能力,按招考录用计划择优录用。因此,考试具有较高的信度、效度、区分度和一定的难度。
二、考试形式与考试结构
考试形式:闭卷,笔试。“专业知识”满分100分,考试用时100分钟;“教法技能”满分50分,考试用时50分钟。二者合卷满分共150分,考试限定用时150分钟。
试题类型:“专业知识”的题型为单项选择题、填空题、简答题、推导题、计算题;“教法技能”的题型为单项选择题、填空题、简述题、简答题、教学设计题。
三、考试内容
专业知识
以现行大学师范类化学教育专业本科主干课程《无机化学》、《有机化学》和普通高中《化学课程标准》、《中学化学教学法》为依据,综合高中知识,突出大学本科师范类化学教育专业上述主干课程的主要内容,以高中化学教师应具备的教育教学水平和能力要求为重点确定考试内容。
无机化学部分
1.一些化学基本概念和定律
(1)化学有关基本概念(原子、分子、元素、核素、同位素、相对原子质量……)等;
(2)“物质的量”及其单位——摩尔的概念及计算;
(3)理想气体状态方程及应用条件;
(4)分压定律及有关概念。
2.化学平衡
(1)化学平衡的概念,平衡常数及意义;
(2)多重平衡规则;
(3)有关化学平衡的计算;
(4)化学平衡移动原理及应用。
3.电离平衡
(1)酸碱电离理论和酸碱质子理论;
(2)PH的意义及PH与氢离子浓度的相互换算;
(3)同离子效应,盐效应;
(4)缓冲溶液的组成、原理及计算;
(5)Ksp的意义及溶度积规则;溶度积Ksp与摩尔溶解度(S)的关系、换算及沉淀溶解平衡有关计算。
4.化学反应速度
(1)化学反应速度及表示方法;
(2)两种反应速度理论——碰撞理论和过渡状态理论及应用。
5.化学热力学初步
(1)状态函数U、H、S、G、△U、△S、△H、△G、△ƒHo、△ƒGo和So的概念、意义和性质;
(2)热力学第一定律和盖斯定律及计算;用△ƒHo、△ƒGo和So求算标准状态和非标准状态下体系的△Ho、△So和△Go(△G);
(3)吉布斯一赫姆霍兹公式及意义,△G与△H和△S的关系,并会用于分析温度对化学反应自发性的影响;
(4)吉一赫公式的计算和应用, 反应自发进行最低温度的计算;
(5)化学反应等温式的意义和用途,公式:△Go=–TRlnK 的应用。
6.原子结构和元素周期系
(1)原子结构有关术语和概念;
(2)四个量子数n、l、m、ms的意义、取值和相互关系;
(3)用四个量子数写出1—4周期常见元素的电子结构式;相反,由结构式确定元素所在周期、族、区、特征电子构型(即价电子构型)、元素名称和高氧化态及低氧化态化合物化学式;
(4)原子结构与周期系的关系。
7.分子结构
(1)化学键参数有关基本概念和分子的性质(极性、磁性);
(2)离子键和共价键的基本特性及其区别;
(3)共价键理论、杂化轨道理论及分子轨道理论;
(4)分子间力和氢键;
(5)晶体的四种基本类型和特点。
8.氧化还原反应
(1)氧化还原有关基本概念和方程式配平(包括氧化数法—离子~电子法);
(2)理解电极电势(φ0)的意义,用φ0判断氧化剂、还原剂的强弱,选择适当的氧化、还原剂;
(3)用φ0计算并判断氧化还原反应方向和程度(公式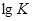 =
=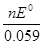 );
);
(4)标准元素电势图及应用;
(5)能斯特方程及应用。
9.配位化合物
(1)配合物有关基本概念;
(2)配合物的命名;
(3)用杂化轨道理论讨论常见配合物的杂化类型及对其性质的影响;
(4)配合物稳定常数(K稳)的意义及应用。
10.元素部分
(1)主族元素、副族元素的特性;
(2)金属通性,掌握元素之最(例如:最轻的气体、地壳中含量最高的元素,比重最大的金属,硬度最大的金属……);
(3)常见元素氯、溴、碘、氧、硫、氮、磷、碳、硅、硼、铝、铜、银、锌、汞、铬、锰、铁、钴、镍单质和重要化合物的结构和性质;
(4)“缺电子原子”、“等电子原子”、“缺电子化合物”、“等电子体”、“惰性电子对效应”、“大兀键”、“桥键”等基本概念及实例;
(5)常见无机物的结构、性质,掌握常见化学试剂的俗名。
有机化学部分
1.烷烃:掌握有机化合物的分类、命名原则;理解б键的定义及特点;了解烷烃构型、物理性质及变化规律;掌握卤代反应—游离基反应的基本历程;理解烷的氧化、裂解反应。
2.烯烃:熟练掌握烯烃的系统命名法、Z/E、顺/反命名法;理解sp2杂化及п键定义、特点;认识加成反应特点,理解离子型亲电加成反应;掌握马氏规则及过氧化物效应;掌握烯烃的鉴别方法;掌握烯烃的制备方法;了解烯烃的几个重要反应及在生产中的应用。
3.炔烃 二烯烃:掌握炔烃、二烯烃的命名方法,sp杂化特点;掌握炔烃的性质(加成、聚合、氧化);掌握共轭二烯烃的结构特点及重要性质;掌握炔烃的鉴别方法;理解共轭效应定义及特点。
4.脂环烃:熟练掌握脂环烃命名方法;掌握环烷烃的结构特点;掌握环烷烃性质特别是小环烷烃的性质。
5.芳烃:熟练掌握芳烃的命名方法;理解苯环结构、特征;掌握苯及同系物的化学性质;掌握亲电取代反应历程、定位规则、定位规则的应用;掌握芳烃的鉴别方法。
6.多环芳烃和非苯芳烃:了解联苯的命名及性质;掌握稠环芳烃的命名、结构及性质;理解非苯芳烃的概念及休克尔规则。
7.立体化学:掌握立体异构、光学异构、对称因素、手性碳、对映体、非对映体、外消旋体、内消旋体、比旋光度等基本概念;掌握Fischer投影式书写方法、D、L命名法和R、S命名法。
8.卤代烃:熟练掌握卤代烃的化学性质及结构与性质间关系;掌握亲核取代反应历程、消除反应历程; 掌握卤代烃的制备方法;认识几种常见卤代烷、卤代烯烃、卤代芳烃、多卤代烃的性质及用途。
9.醇和醚:掌握醇、醚的命名、结构特点及化学性质的差异;掌握醇、醚的基本反应与鉴别方法;熟悉主要的醇、醚的制备方法。
10.酚和醌:掌握酚的结构、命名及制法;掌握酚的化学性质及酚的鉴别方法。
11.醛和酮:掌握碳氧双键和碳碳双键的结构差异及在加成反应方面的异同;熟练掌握醛、酮的化学性质,重点是亲核加成反应,理解其反应历程;掌握醛、酮在化学性质上的差异,如氧化还原反应及歧化反应;掌握醛酮的鉴别方法。
12.羧酸及其衍生物:掌握羧酸及羧酸衍生物的系统命名法及常见羧酸的俗名;熟练掌握羧酸的化学性质;掌握诱导效应和共轭效应对羧酸性质的影响;了解羧酸及羧酸衍生物的制备方法;掌握羟基酸命名及性质;熟练掌握羧酸衍生物的化学性质及它们之间的相互转化关系;熟练掌握丙二酸酯、乙酰乙酸乙酯在合成上的应用。
13.硝基化合物和胺:了解硝基化合物的结构、性质;掌握胺的分类、命名、结构;掌握胺的性质及碱性强弱顺序;了解区别伯、仲、叔胺的方法及重要的胺;掌握重氮盐的反应和偶合反应在有机合成中的应用。
14.重氮化合物和偶氮化合物:掌握重氮化反应;掌握重氮盐性质及其在合成中的应用。
15.杂环化合物:掌握杂环化合物的分类、命名;理解杂环化合物的结构与芳香性;掌握五员杂环化合物的性质;掌握六员杂环化合物的性质。
教法技能(化学教学)
1.《普通高中课程方案》:普通高中的培养目标,课程结构,课程内容选择的原则。
2.《普通高中化学课程标准》:①普通高中化学课程性质,课程的基本理念,课程设计思路。②课程目标。③内容标准。④实施建议。
3.从课程目标的三个维度来设计教学过程;提高科学探究的质量,关注科学探究学习目标的达成;化学贴近生活、联系社会生产、生活实际;突出化学学科特点,发挥实验在化学教学中的重要作用。
4.化学教学基本功:组织教材的基本功;设计科学探究和化学实验的基本功;应用化学知识解决实际问题的基本功;组织教学的基本功;化学教学评价命题的基本功;参与化学教学研究的基本功;课程资源的开发和利用的基本功。
5.制定化学教学中的学年(期)、单元、章节、课时教学计划;依据教学内容和学生实际备课、上课、辅导、批改作业、学生成绩考核;教学设计、编写教案、学案、说课案。
四、考试要求
无机化学部分
1.一些化学基本概念和定律
(1)了解本章有关化学基本概念(原子、分子、元素、核素、同位素、相对原子质量……);
(2)掌握“物质的量”的意义及其单位—摩尔的概念,能熟练应用并进行有关计算;
(3)掌握理想气体状态方程及应用条件;
(4)了解分压定律及有关概念。
2.化学平衡
(1)掌握化学平衡的概念,理解平衡常数及意义;
(2)掌握多重平衡规则;
(3)掌握有关化学平衡的计算;
(4)掌握化学平衡移动原理及应用。
3.电离平衡
(1)了解酸碱理论的发展概况,掌握酸碱电离和酸碱质子理论;
(2)掌握PH的意义、PH与氢离子浓度的相互换算;
(3)掌握同离子效应,盐效应的概念及应用;
(4)了解缓冲溶液的组成、原理,掌握缓冲溶液PH值的计算;
(5)掌握Ksp的意义及溶度积规则:掌握Ksp与摩尔溶解度(S)的关系、换算及沉淀
溶解平衡有关计算。
4.化学反应速度
(1)掌握化学反应速度的表示方法;
(2) 熟悉两种反应速度理论——碰撞理论和过渡状态理论,会用活化分子、活化能(Ea概念解释T、C(P)和催化剂对反应速度的影响。
5.化学热力学初步
(1)掌握状态函数 U、H、S、G、△U、△S、△H、△G、△ƒHo、△ƒGo和So的概念和性质;
(2)掌握热力学第一律和盖斯定律及计算;掌握用△ƒHo、△ƒGo和So求算标准状态和非标准状态下体系的△Ho、△So和△Go(△G)的方法;
(3)掌握吉布斯一赫姆霍兹公式及意义,掌握△G与△H和△S的关系,并会用于分析温度对化学反应自发性的影响;
(4)掌握吉布斯一赫姆霍兹公式的计算和应用,会用其判断反应自发进行的方向、程度,会求反应自发进行的最低温度;
(5)了解化学反应等温式的意义和用途,会用公式:△Go=–TRlnK 求算反应的△G和K(平衡常数)。
6.原子结构和元素周期系
(1)了解原子结构有关术语和概念;
(2)掌握四个量子数n、l、m、ms的意义、取值和相互关系;
(3)会用四个量子数写出1—4周期常见元素的电子结构式;相反,由结构式确定元素所在周期、族、区、特征电子构型(即价电子构型)、元素名称和高氧化态及低氧化态化合物化学式;
(4)掌握原子结构与周期系的关系。
7.分子结构和晶体结构
(1)了解化学键参数有关基本概念和分子的性质;
(2)会根据化学键和分子结构判断分子是否有极性;
(3)掌握离子键和共价键的基本特性以及它们的区别;
(4)掌握共价键理论、杂化轨道理论,了解分子轨道理论,会用上述理论确定常见共价小分子的杂化类型和基本性质;
(5)掌握分子间力和氢键的概念和应用;
(6)掌握晶体的四种基本类型和特点。
8.氧化还原反应
(1)掌握氧化还原有关基本概念和方程式配平(包括氧化数法和离子~电子法);
(2)理解电极电势(φ0)的意义,会用φ0判断氧化剂、还原剂的强弱,选择适当的氧化、还原剂;
(3)掌握用φ0计算并判断氧化还原反应方向和程度的方法(用公式lgK=);
(4)掌握用准标元素电势图判断歧化反应及其反应程度的计算;
(5)了解能斯特方程及应用。
9.配位化合物
(1)了解配合物有关基本概念;
(2)掌握配合物的命名;
(3)掌握用杂化轨道理论判断常见配合物杂化类型、分子构型、稳定性、磁性等性质的方法;
(4)理解配合物稳定常数(K稳)的意义,掌握应用K稳计算并判断配位离解反应方向、限度,配离子生成和破坏的方法。
10.元素部分
(1)掌握主族元素、副族元素的特性;
(2)了解金属通性,掌握元素之最(例如:最轻的气体、地壳中含量最高的元素,比重最大的金属,硬度最大的金属……);
(3)掌握常见元素卤素、氧、硫、氮、磷、碳、硅、硼、铝、铜、银、锌、汞、铬、锰、铁、钴、镍单质和重要化合物的结构和性质;
(4)掌握“缺电子原子”、“等电子原子”、“缺电子化合物”、“等电子体”、“惰性电子对效应”、“大兀键”、“桥键”等基本概念及实例;
(5)了解常见无机物的结构、性质,掌握常见化学试剂的俗名。
有机化学部分
1.考核考生掌握有机化合物的命名、主要性质、有机化合物的主要合成方法;
2.考察考生应用有机分子基本反应类型及主要官能团的特性和相互转化规律的能力。
教法技能(化学教学)
1.了解《普通高中课程方案(实验)》的主要内容:普通高中教育的培养目标,课程结构,课程内容选择的原则。
2.了解普通高中《化学课程标准》的主要内容,明确化学学科在高中教学中的地位和作用;明确各模块内容间的关系和各模块内容的地位和作用。
3.掌握高中化学教育的基本原则和基本方法。
4.能够创设情景激发学生学习化学的兴趣;把握好课堂教学结构,选择适当的教学方法进行教学设计,进行实际教学。
5.掌握科学探究和化学实验能力的要求,明确科学探究要素。
6.依据《化学课程标准》、教学内容和教学要求,正确、科学地评价学生学业成绩,指导学生学习,促进学生发展。
五、题型示例
专业知识
一、单项选择题(本大题共15个小题,每小题2分,共30分)
1.食品干燥剂应无毒、无味、无腐蚀性以及对环境友好。下列说法错误的是
A.硅胶可用作食品干燥剂
B.P2O5不可用作食品干燥剂
C.六水合氯化钙可用作食品干燥剂
D.加工后具有吸水性的植物纤维可用作食品干燥剂
2.已知公式 的 ,则此反应
的 ,则此反应
A.低温下是自发变化 B.高温下是自发进行
C.低温下是非自发变化,高温下是自发变化 D.任何温度下都是非自发进行
3.ψ(3, 2, 1) 代表简并轨道中的一条轨道是
A.2p 轨道 B.3p 轨道 C.3d 轨道 D.4f 轨道
4.下列元素原子半径的排列顺序正确的是
A.Mg > B > Si > Ar B.Ar > Mg > Si > B
C.Si > Mg > B > Ar D.B > Mg > Ar > Si
5.欲配制pH=5.0左右的缓冲溶液,可选用的缓冲体系有

6.下列配合物中,配位数最大的是
A.[Cu(Cl)4]2- B.[Cu(EDTA)]2- C.[AgCl2]- D.[Cu(en)2]2+
7.电极电势与pH无关的电对是
A.H2O2/H2O B.IO3/I- C.MnO2/Mn2+ D.MnO4-/MnO42-
8. 加入水中能抑制水的电离的物质是
A.碘化钾 B.氯化钠 C.硝酸钠 D.硫酸
9.密闭容器中反应CO(g)+H2O(g) CO2(g)+H2(g)+Q(Q>0)达到平衡,在其他条件不变的情况下,下列措施不能使正反应速率加快的是
CO2(g)+H2(g)+Q(Q>0)达到平衡,在其他条件不变的情况下,下列措施不能使正反应速率加快的是
A.通入水蒸气 B.缩小容器体积 C.分离出CO2 D.升高温度
10.分离苯和水,应选用的装置是
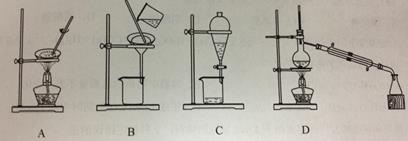
11.下列说法正确的是
A.仅用AgNO3溶液便可鉴别亚硝酸钠和食盐
B.重结晶时,溶液冷却速度越慢得到的晶体颗粒越大
C.乙酸与乙醇的混合液可用分液漏斗进行分离
D.用标准盐酸滴定待测NaOH溶液时,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低
12.下列化合物能发生歧化反应的是
A . CH3CH2CHO B. CH3COCH2CH3 C . C6H5CHO D. (CH3)2CHCHO
13.一定温度下的密闭容器中发生可逆反应C(s) + H2O(g)CO(g) + H2(g),一定能说明该反应已达到平衡状态的是
A.v逆(H2O)=v正(CO) B.容器中物质的总质量不发生变化
C.n(H2O) : n(H2)=1 : 1 D.生成1molCO的同时生成1molH2
14.将CH3CH=CHCHO氧化成CH3CH=CHCOOH选择下列哪种试剂较好?
A. 酸性KMnO4 B. 托伦斯试剂 C. K2Cr2O7 + H2SO4 D. HNO3
15.下列化合物能发生碘仿反应的是
A. 2-甲基丁醛 B. 异丙醇 C. 3-戊酮 D. 丙醇
二、填空题(本大题共 11个小题,每空1分,共20分)
16.已知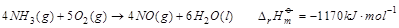
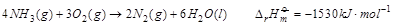 则NO的摩尔生成焓为 。
则NO的摩尔生成焓为 。
17.基元反应2NO + Cl2 2NOCl的总反应级数是 。
2NOCl的总反应级数是 。
18.某元素核外电子排布式为>1s22s22p63s23p5,则该元素的原子序数为 ,元素符号为 ,属于 周期, 族。
19.在K2MnO4 中,Mn的氧化数为 。氧化还原电对的电极电势越负,该电对的还原型的 能力越强。
20.一般不用玻璃容器盛HF溶液的原因是 。
21.所有金属中,地壳中含量最高的是 ,常温常压下只有 是液体。
22. 分馏装置中分馏部分由蒸馏瓶、_____________、温度计、____________及____________等组成。
23. 某烯烃A是有机化学工业的基本原料,其相对分子质量为28,A可发生如下图所示的一系列化学反应(部分产物已略去),其中反应①②③均属于加成反应。
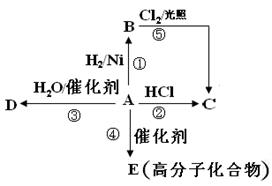
请回答下列问题:
(1)写出D的结构简式 。
(2)写出④的反应类型 。
(3)写出②的化学方程式 。
24. 完成反应式: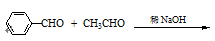 。
。
25. 用系统命名法命名化合物 :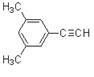 ________________________。
________________________。
26. 用格氏试剂制备1-苯基-2-丙醇,最好采用下列哪种方案_________(选填编号)。
A. CH3CHO + C6H5CH2MgBr B. C6H5CH2CH2MgBr + HCHO
C. C6H5MgBr + CH3CH2CHO D. C6H5MgBr + CH3COCH3
三、简答题(本大题共9个小题,共25分)
27.(4分)根据杂化轨道理论或价电子对互斥理论判断:
| 分子 | 杂化方式 | 分子的空间构型 | 配离子 | 杂化方式 | 配离子的空间构型 |
| [FeF6]2- |
28.(3分)HF的沸点比相应的同族元素氢化物的沸点反常的高,为什么?
29.(3分)SO2与Cl2的漂白作用有什么不同?
30.(2分)写出苄醇的结构式。
31.(2分)用反应式表示过氧化物效应。
32.(2分)用结构式表示p-π共轭体系。
33.(2分)比较下列羰基化合物与NaHSO3加成反应的快慢:(由快到慢)
A. 苯乙酮 B. 苯甲醛 C. 2-氯乙醛 D. 乙醛
34. (3分)用化学方法鉴别1,2-丙二醇,正丁醇, 甲丙醚, 溴代环己烷。
35. (4分)以小于等于四个碳的烃合成乙基叔丁基醚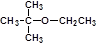
四、推导题(根据题目所给条件推导化合物结构。本大题共3个小题,共15分)
36.(5分)在溶液A中加入AgNO3溶液,会析出白色沉淀,该白色沉淀可溶于氨水得到无色溶液B,向B中加入KI,生成黄色沉淀AgI。将H2S通入溶液A中,产生褐色沉淀C,沉淀C可溶于Na2S2,形成溶液。在HgCl2溶液中加入少量的溶液A得到白色沉淀D,继续加入溶液A,沉淀D逐渐变灰,最后变为黑色沉淀E。写出A、B、C、D、E所代表的物质的化学式。
37.(4分)分子式为C5H12O的A,能与金属钠作用放出氢气,A与浓H2SO4共热生成B。用冷的碱性高锰酸钾水溶液处理B得到产物C。C与高碘酸作用得到CH3COCH3及
CH3CHO。B与HBr作用得到D(C5H11Br),将D与稀碱共热又得到A。推测A、B、C的结构。
38.(6分)化合物A(C11H14O2),用酸处理得到B (C8H8O2)和C(C3H8O),B呈酸性,C可以发生碘仿反应,B用高锰酸钾或重铬酸钾处理得D(C8H6O4),D可用对二甲苯制得,写出A、B、C、D的结构式。
五、计算题(本题10分)
39.(10分) 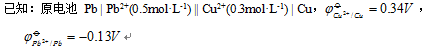
(1) 写出电极反应式及电池反应方程式;
(2) 计算上述原电池的电池电动势E;
(3) 计算298K时反应的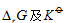 。
。
教法技能(化学教学)
一、单项选择题(本大题共 4个小题,每小题3分,共12分)
1.《普通高中化学课程标准》体现时代性、基础性和
A. 发展性 B. 启蒙性 C. 选择性 D. 创新性
2. 课程标准的内容包括四个部分,对化学课程性质论述的部分是
A.前言部分 B. 课程目标部分 C. 内容标准部分 D. 活动与探究建议部分
3. 学生在学习“电离平衡”概念之前已经学习了“化学平衡”的有关知识,据此,我们可以优选( )策略来帮助学生学习电离平衡。
A. 概念形成 B. 概念同化
C. 概念图 D. 多重联系
4. 既评价学生的过程表现,又评价学生的学习结果的评价方式是
A. 学生互评 B. 学生自评 C. 书面测验 D. 活动表现评价
二、填空题(本大题共 3个小题,每空1分,共11分)
5. 化学新课程构建了以提高学生科学素养为主旨的目标体系,这个体系由 、
、 三个维度的目标构成。
6. 中学化学课程标准的作用是 、 和 。
7. 中学化学教育研究的基本环节是: 、 、
、 、 。
三、简答题 (本大题共 2个小题,每小题6分,共12分)
8. 请结合实际简述使化学教学内容更加贴近生活、贴近社会的教学实施策略。
9. 请你举实例来说明在化学教学中如何培养学生的想象力。
四、教学设计题(本题15分)
10. 以人教版高中教材必修1第四章第二节部分内容——“氯气的性质”。请结合教材编写“氯气的性质”的教学目标,并设计一段教学情景,引入新课。
参考书目:
1.《普通高中课程方案(实验)》,中华人民共和国教育部制订,人民教育出版社出版。
2.普通高中《化学课程标准(实验)》,中华人民共和国教育部制订,人民教育出版社出版。
3.现行普通高中化学教科书。
4.高等师范院校(本科)相关教材。


